
提问:你是天生自带“早起开关”的晨型人,还是越到深夜越清醒的夜猫子?
如今,很多人都被起床困难、入睡拖延反复困扰。大家是否也羡慕这样一群人:Ta们每天只睡4–6小时,却依旧精力充沛、思路清晰?
长久以来,我们习惯于将作息偏好的差异归因于生活习惯的优劣或自律程度的高低。例如,那些事业有成的成功人士,似乎总能在极短的睡眠后依然活力满满,而另一边,熬夜、睡不醒的人则常被贴上“懒惰”或“自制力差”的标签。但如今,科学家们却发现:一个人的昼夜节律、作息类型,很大程度上,早已写进了基因里!
基因决定你是 “早鸟” 还是 “夜猫子”
近日,国际顶级期刊Nature Communications发表了题为“Genome-wide association analyses of chronotype in 697,828 individuals provides insights into circadian rhythms”的研究论文,该文章基于一项迄今规模最大的睡眠类型基因组研究,对697,828 人进行全基因组关联分析(GWAS),一举将与 “早起型” 相关的基因位点从 24 个扩充至351 个,首次用客观数据证实:作息偏好由基因主导,且直接影响心理健康。

DOI: 10.1038/s41467-018-08259-7
该研究整合了英国生物银行(UK Biobank)与 23andMe 的超大队列数据,研究发现:351 个基因位点与作息偏好强相关,值得说明的是,相比此前研究仅发现 24 个位点,本次新增327 个全新基因位点,覆盖大量核心生物钟调控基因,包括PER1、PER2、PER3、CRY1、ARNTL等经典节律基因。
随后,研究团队基于85760名佩戴运动手环人群的客观睡眠数据展开验证。结果显示,携带“早起等位基因”最多的前5%人群,平均入睡与起床时间,比携带该基因最少的人群足足早了25分钟。
更有意思的是,这类基因只决定你“几点睡”,并不决定你“睡多久”。这些基因位点仅对睡眠时段具有特异性调控作用,对睡眠时长、睡眠效率及睡眠碎片化程度等均无显著影响。
简单来说:是天生“早鸟”还是“夜猫子”,由基因说了算;但睡够多长时间,与它们无关。
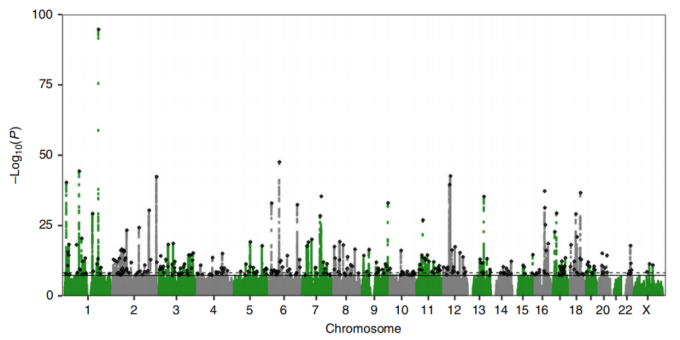
时型荟萃分析全基因组关联研究(GWAS)曼哈顿图
那么,这些基因具体是如何影响我们作息的?研究者从两个层面找到了线索。
首先,通过通路富集与组织表达分析,研究者发现,影响昼夜节律偏好的核心调控区域,集中在下丘脑视交叉上核(SCN,即人体生物钟“司令部”)、视网膜、后脑及垂体,这些区域均高度富集节律调控基因。
接着,研究者锁定了几条关键信号通路:cAMP信号通路、谷氨酸信号通路、胰岛素信号通路,以及参与时钟蛋白降解调控的泛素-蛋白酶体通路。
值得一提的是,光感知在节律调节中扮演着关键角色。视网膜光信号传导相关基因(如RGS16、INADL)的变异,会直接影响人体生物钟与外界光照的同步能力。这也从根本上解释了:为何有些人天一亮便能自然清醒,而有些人即便熬夜后补觉,第二天也依旧会精神昏沉。
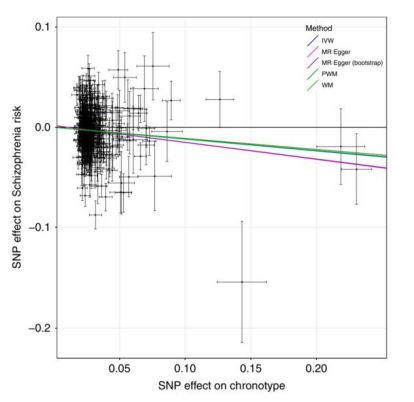
精神分裂症发病风险与作息表型暴露的孟德尔随机化散点图
而这项研究最具临床意义的突破在于:首次证实作息类型对心理健康存在因果性影响。研究者运用孟德尔随机化方法,有效排除了“熬夜是因为抑郁”或“生活习惯导致两者相关”等混杂因素的干扰,得出明确结论:
早起型人群整体心理健康水平更佳,主观幸福感显著更高;
精神分裂症发病风险显著降低;
抑郁症状及重度抑郁风险也呈现明显下降趋势。
由此可见,“夜猫子”并非单纯的生活习惯选择,而是由部分基因决定的先天易感性。晚间型人群更高的抑郁及精神健康风险,也并非仅仅因为“熬夜伤身”,而是有其深刻的生物学根源——这种风险,很大程度上由影响作息类型的基因本身因果驱动。
人类“短睡基因”再添实锤!
如果说上面这些基因决定的是我们“什么时候睡”,那接下来的发现则告诉我们:有人天生“不需要睡那么久”。
你身边有没有这样的人?每天只睡四五个小时,却精神抖擞、精力充沛,甚至“睡多了反而难受”?在科学上,这种特质被称为“自然短睡眠”——这群人并非睡眠不足,而是天生就不需要那么多睡眠。
那么,究竟是什么让他们如此“高效”地完成睡眠?一项最新发表在PNAS期刊上的研究,科学家首次证实人类盐诱导激酶 3(SIK3)基因的 N783Y 突变,是导致天然短睡眠(NSS)的关键原因。携带这一突变的人群,无需长时间睡眠就能维持正常生理功能,且没有慢性睡眠不足带来的健康隐患。

DOI: 10.1073/pnas.2500356122
这一次,研究团队在一个家族性短睡家系中,发现了一名70多岁的健康老人。他自我报告每天仅睡3小时,客观监测显示平均睡眠6.3小时。全外显子测序锁定了SIK3-N783Y突变——一种极为罕见的基因变异。
这个突变到底做了什么?
体外实验表明,N783Y突变显著降低了SIK3对底物蛋白的磷酸化能力。换句话说,这个突变让SIK3的“工作强度”降低了,是一种功能丧失型突变。
为了验证这个突变是否真的能导致短睡,研究团队构建了携带同样突变的小鼠模型。在12小时光照/12小时黑暗的周期下,携带N783Y突变的小鼠,每天的睡眠时间比正常小鼠减少了约31.8分钟,尤其是在活跃期(暗光期)睡眠显著减少。虽然减少的时间看似不多,但在小鼠这种睡眠本就碎片化的动物中,这是一个显著的变化。
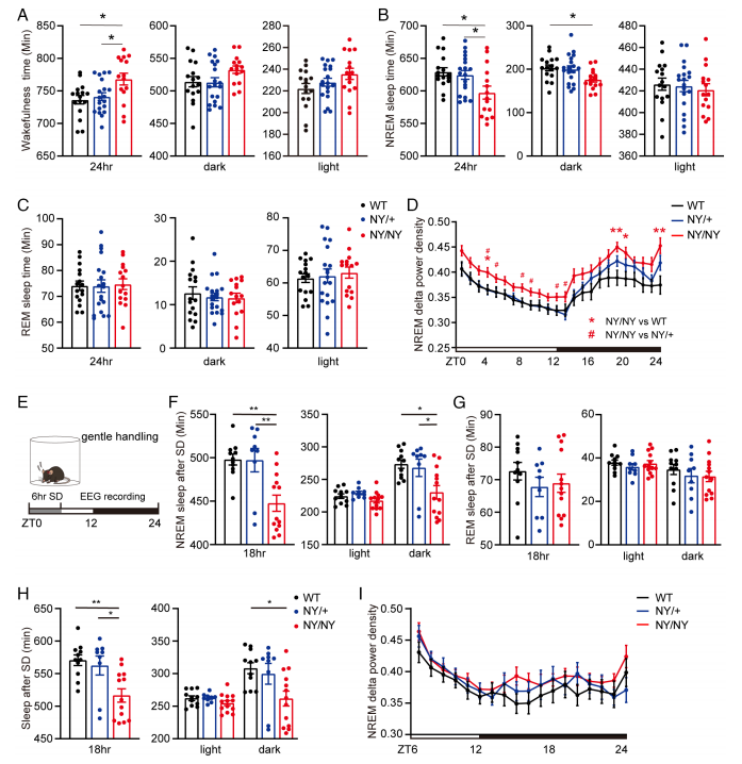
Sik3-N783Y小鼠表现出睡眠时间缩短
更值得注意的是,在经历6小时的睡眠剥夺后,突变小鼠的“补觉”时间也比正常小鼠少了约54分钟,这说明它们确实对睡眠的需求降低了。
那么,突变是如何影响大脑的?
研究人员对小鼠大脑前脑组织进行了定量磷酸化蛋白质组学分析,结果发现:突变小鼠脑内782个磷酸化位点发生了显著变化,其中大多数是磷酸化水平下降。这些变化主要集中在突触部位,也就是神经元之间传递信息的关键结构。而突触蛋白的磷酸化状态,正是调控睡眠-觉醒节律的重要机制之一。
进一步分析表明,SIK3可能通过调控蛋白激酶A(PKA) 和丝裂原活化蛋白激酶(MAPK) 等信号通路,形成一个复杂的激酶网络,共同决定睡眠时长和质量。这也为未来开发调节睡眠的药物提供了新的潜在靶点。
神奇基因曝光!让人每天只睡4小时还精力爆棚的秘密
无独有偶,另一支研究团队从不同的短睡家族中,锁定了另一个关键基因——GRM1。它和SIK3一样,都能让人“睡得更少却精神更好”,但作用的分子机制却截然不同。
这项发表在《当代生物学》上的研究发现,GRM1基因的两个独立失功能突变,是导致家族性自然短睡眠的另一重要原因。

DOI: 10.1016/j.cub.2020.09.071
GRM1编码的是一种叫做“代谢型谷氨酸受体1”的蛋白,它在大脑中扮演“刹车”的角色,负责抑制过度的神经信号。而这两个突变,一个位于受体的“头部”(与外界信号结合的区域),一个位于“尾巴”(与细胞内信号传导相关的区域),但殊途同归,都让这个“刹车”失灵了。
研究人员借助基因编辑技术,将这两种突变分别导入小鼠体内。结果令人振奋:携带突变的小鼠,每天睡眠时间平均减少约25分钟——这一变化在小鼠身上已相当显著。睡眠减少主要集中在非快速眼动睡眠阶段,深度睡眠基本不受影响;小鼠日间状态正常,即便经历睡眠剥夺,也能正常完成睡眠补偿。
那么,这个“刹车失灵”是怎么让人睡得更少的?
进一步机制探索发现,突变小鼠脑中特定神经元(尤其海马区)的兴奋性明显升高:本该被抑制的神经信号难以平静,神经元间的信号传递变得更活跃、更高效。这或许就是它们无需长时间睡眠,也能维持高效清醒状态的关键原因。
这一发现意义重大。GRM1成为了继DEC2、ADRB1、SIK3之后,又一个被“实锤”的人类短睡基因。 更重要的是,携带这类突变的人群身体健康、无任何不良后果——这提示我们,睡眠调控存在灵活的“安全区间”,并非人人都必须睡满8小时才算健康。
小结
综上所述,我们每个人的睡眠模式,其实早就在基因里写好了“出厂设置”。有些人就是天生适合并且擅长早睡早起,到点就困,天亮就醒;有些人则自带“夜猫子”体质,越晚越精神,早上起床困难;有些人睡够八小时才满血复活;有些人睡五六个小时照样神采奕奕。
总之,只要你有属于自己的稳定节奏,醒来神清气爽、白天精力在线、做事不昏沉,那就是最适合你的、最好的睡眠啦~
参考文献: [1] Jones SE, Lane JM, Wood AR, et al. Genome-wide association analyses of chronotype in 697,828 individuals provides insights into circadian rhythms. Nat Commun. 2019 Jan 29;10(1):343. [2] Chen H, Xing Y, Wan C, et al. The SIK3-N783Y mutation is associated with the human natural short sleep trait. Proc Natl Acad Sci U S A. 2025 May 13;122(19):e2500356122. [3] Shi G, Yin C, Fan Z, et al. Mutations in Metabotropic Glutamate Receptor 1 Contribute to Natural Short Sleep Trait. Curr Biol. 2021 Jan 11;31(1):13-24.e4
原标题:不是不愿意起,是真的起不来!多项研究:作息偏好由基因主导,且作息类型对心理健康存在因果性影响
本文作者:青叶,转载于微信公众号:生物谷(ID:BIOONNEWS),转载引用请注明原出处