
我们都知道熬夜伤身,但到底伤在哪里、有没有办法补救,科学界一直在寻找答案。最近,来自江南大学的研究团队发表于Food & Function的一项研究表明,熬夜的伤害可以逆转。研究团队发现一种名为长双歧杆菌CCFM1238的益生菌,能够通过调节生物钟基因、改善肠道菌群,显著缓解睡眠不足导致的肠道炎症和认知损伤。

DOI:10.1039/d5fo02921j
熬夜,不仅仅是“困”这么简单
我们每个人都有一套精密的“生物钟系统”,它由一系列时钟基因(如Bmal1、Clock、Per3、Cry1、Rev-erbα等)调控,管理着睡眠、饮食、代谢等多种生理活动的昼夜节律。一旦因为熬夜、轮班、跨时区旅行等原因导致生物钟紊乱,身体就容易出现各种问题。
全球约1/3的人受睡眠问题困扰,长期睡眠不足不仅会引发焦虑、抑郁等情绪障碍,还会导致肠道屏障受损、炎症反应加剧,甚至影响记忆力和学习能力。
目前,对付失眠或节律紊乱常用一些特定的药物,但长期使用的安全性和依赖性令人担忧。因此,研究者们一直在寻找更安全、可持续的调节方式。近年来,“肠-脑轴”理论备受关注,肠道菌群被称为人体的“第二大脑”,它们本身也有昼夜节律,并与宿主生物钟相互影响。一些研究发现,补充特定益生菌可以改善睡眠质量、缓解情绪压力,但其具体作用机制和菌株筛选方法仍不明确。
如何从海量益生菌中找出“时钟调节员”?
江南大学团队决定攻克这个难题。他们首先面临一个现实问题:益生菌种类繁多,如果直接在动物模型上逐一筛选,成本高、周期长、效率低。于是,他们创新性地建立了一套体外细胞筛选模型,以人源结肠腺癌细胞Caco-2为核心。这种细胞具有类似肠道上皮细胞的特性,且自身表达完整的核心时钟基因,并能维持节律性振荡,非常适合用于模拟肠道局部的生物钟系统。
研究人员从健康人体粪便或发酵食品中分离出10株益生菌,包括长双歧杆菌、短双歧杆菌和植物乳杆菌的不同菌株。他们将细菌或其培养上清液与同步化处理的Caco-2细胞共培养,检测这些益生菌对细胞中5个核心时钟基因表达的影响。
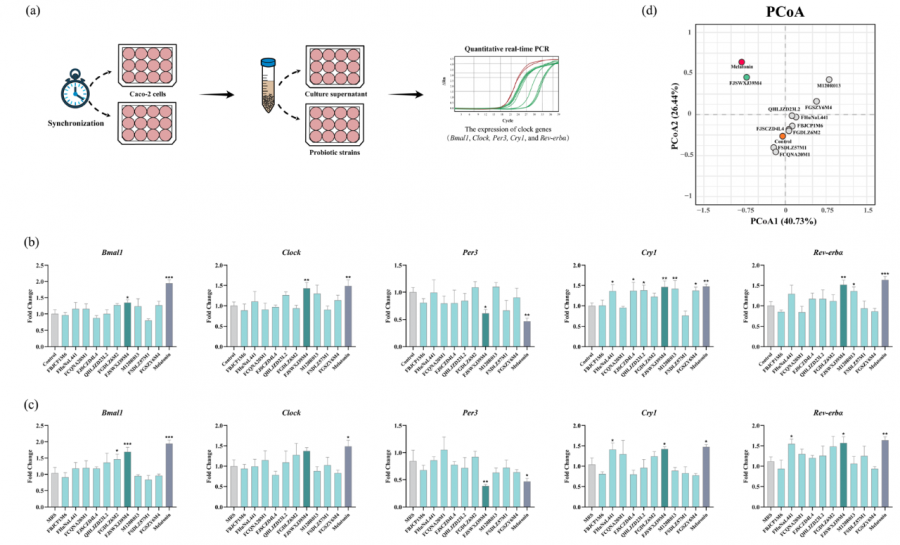
体外筛选具有昼夜节律调节作用益生菌菌株
分析结果表明,长双歧杆菌CCFM1238及其培养上清液表现出最强的节律调节能力,能显著上调Bmal1、Clock、Per3、Cry1和Rev-erbα等多个基因的表达,其调节效果与已知的节律调节剂——褪黑素高度相似。这意味着,CCFM1238在细胞层面就展现出强大的“拨钟”潜力。
细胞实验成功后,研究进入更复杂的动物验证阶段。团队构建了睡眠剥夺小鼠模型,让小鼠连续28天每天只有5小时睡眠,模拟长期熬夜状态。这些小鼠被分为四组:正常对照组、睡眠剥夺组、睡眠剥夺并补充CCFM1238组、睡眠剥夺并补充褪黑素组。
结果表明,睡眠剥夺严重打乱了小鼠肠道和大脑下丘脑的时钟基因节律,并引发了系列病理变化。在肠道中,小鼠回肠的时钟基因表达紊乱,结肠组织出现轻微水肿、炎性细胞浸润,分泌黏液的杯状细胞数量也呈下降趋势,这意味着肠道屏障功能受损。而在大脑中,生物钟中枢下丘脑的基因节律同样失调,海马区的小胶质细胞(大脑中的免疫细胞)被过度激活,这是神经炎症和认知损伤的标志。
补充CCFM1238后,情况得到了显著逆转。在肠道中,它纠正了回肠部分时钟基因的异常表达,减轻了结肠炎症浸润,增加了杯状细胞数量,修复了肠道屏障。在大脑中,它恢复了下丘脑时钟基因的表达节律,并抑制了海马区小胶质细胞的过度活化。这些发现证实,CCFM1238能在活体动物中有效调节中枢和外周生物钟,并减轻相关组织损伤。
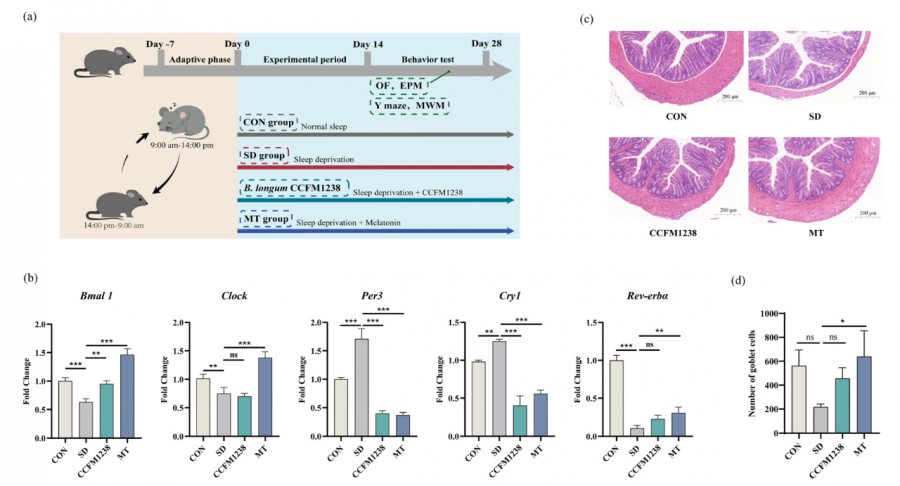
长双歧杆菌CCFM1238改善小鼠睡眠剥夺诱导的肠道节律紊乱和炎症
吃了益生菌,更“聪明”、更“淡定”
光看分子和细胞指标还不够,小鼠的“精神状态”和“智商”有没有改善?研究人员通过一系列经典行为学实验进行了评估。在评估空间学习和记忆的莫里斯水迷宫实验中,睡眠剥夺小鼠寻找隐藏平台的时间明显变长,对目标区域的记忆也更差。而在补充CCFM1238后,小鼠的逃脱时间显著缩短,记忆准确率提升,表现接近正常小鼠。
在评估焦虑情绪的旷场实验和高架十字迷宫实验中,睡眠剥夺小鼠更喜欢待在边缘和安全区域,表现出明显的焦虑样行为。而补充CCFM1238的小鼠则更愿意探索开放的中央区域和开臂,显得更加“淡定”。
在某些测试中,CCFM1238改善焦虑的效果甚至优于褪黑素。这些行为学数据强有力地证明,CCFM1238能够缓解睡眠剥夺导致的认知功能障碍和焦虑样行为。
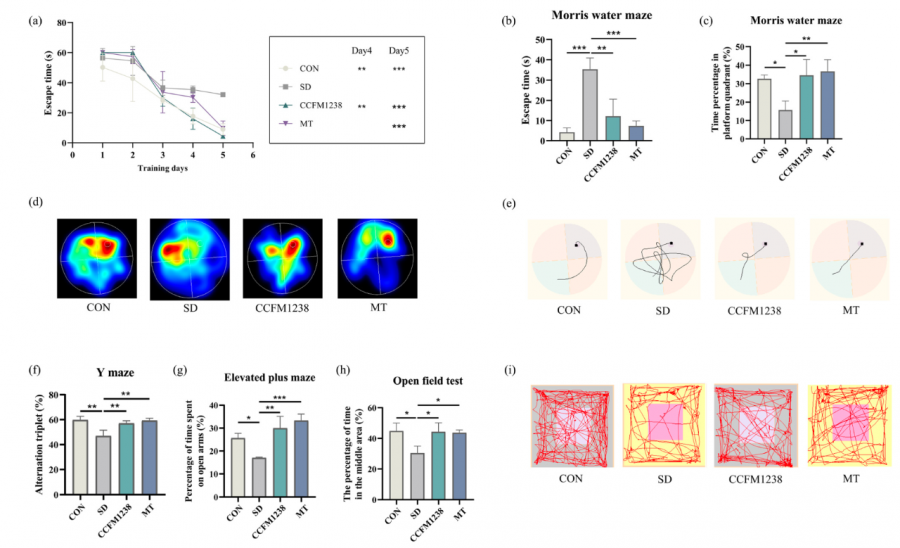
长双歧杆菌CCFM1238改善睡眠剥夺诱导的小鼠认知缺陷
CCFM1238是如何实现“肠-脑同护”的呢?研究团队锁定了肠道微生态。通过对小鼠粪便进行16S rRNA测序,他们发现睡眠剥夺破坏了肠道菌群的平衡,显著增加了菌群的丰富度和均匀度,提高了厚壁菌门与拟杆菌门的比值,这些变化与菌群失调的特征一致。而CCFM1238的干预有效逆转了这些变化,降低了菌群多样性指数,恢复了更健康的菌群结构。
在属水平上,CCFM1238显著提升了阿克曼菌、异杆菌属、双歧杆菌属等有益菌的丰度,同时降低了一些潜在有害菌的丰度。这些有益菌已知与改善肠道屏障、抗炎、产生短链脂肪酸等功能相关。
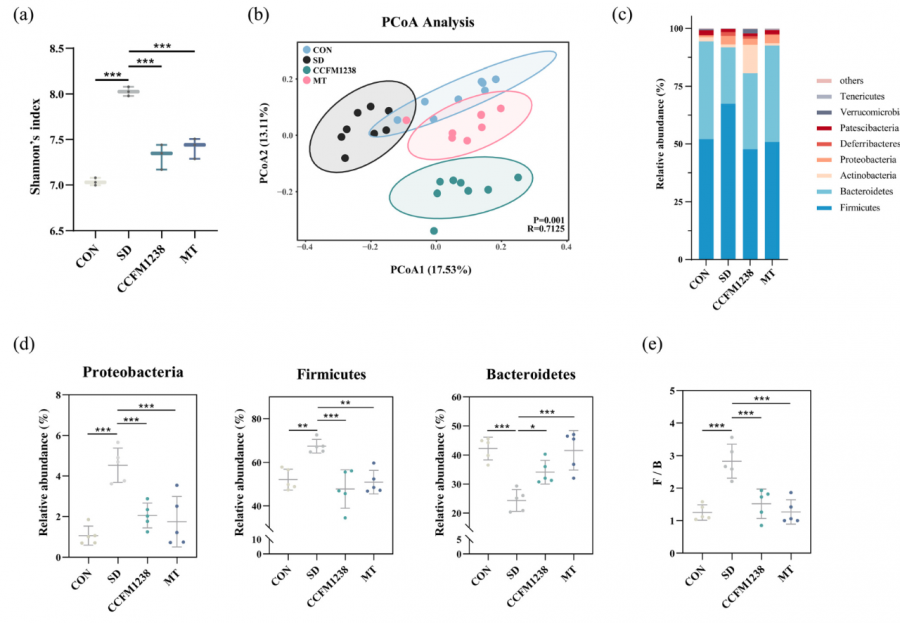
长双歧杆菌CCFM1238调节睡眠剥夺小鼠的肠道菌群
另外,团队通过非靶向代谢组学发现,睡眠剥夺改变了肠道菌群的代谢产物谱,而CCFM1238能特异性地调节一些关键代谢物的水平,例如降低神经毒性物质鞘氨醇,提升腺苷、肌苷、N,N-二甲基甘氨酸等具有神经保护或节律调节功能的代谢物。
进一步的微生物-代谢物关联网络分析揭示,CCFM1238重塑后的有益菌与这些有益代谢物之间存在紧密的正相关关系。例如,神经保护剂肌苷与粪杆菌属丰度正相关,而节律调节剂腺苷则与肠单胞菌属丰度负相关。这说明,CCFM1238很可能通过调控肠道菌群组成,进而影响其代谢产物的输出,这些代谢物作为信号分子,通过肠-脑轴传递,最终调节大脑的生物钟和功能。代谢通路富集分析也显示,嘌呤代谢、苯丙氨酸代谢、牛磺酸代谢等是CCFM1238发挥作用的关键通路。
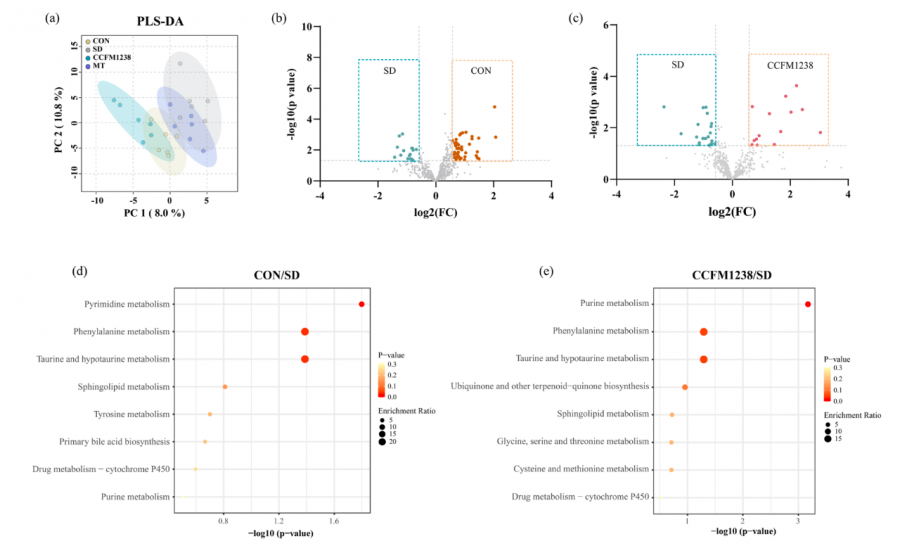
长双歧杆菌CCFM1238调节睡眠剥夺小鼠的肠道菌群代谢物
总的来说,这项研究提示,长双歧杆菌CCFM1238通过其自身或其代谢产物,直接或间接地调节肠道上皮细胞的生物钟基因;同时,它通过重塑肠道菌群生态,增加有益菌、减少有害菌,并促进产生一系列具有神经保护和节律调节功能的代谢物。这些局部和系统的变化共同作用,修复了睡眠剥夺引起的肠道屏障损伤和大脑神经炎症,最终改善了认知和情绪行为。
当然,作者也客观指出了研究的局限性。例如,体外细胞模型无法完全模拟体内复杂的神经内分泌调控网络;动物实验的样本量有限,且仅使用了睡眠剥夺这一种节律紊乱模型;最关键的是,小鼠身上的效果能否在人体中复现,还需要严格的临床试验来验证。
尽管如此,这项研究的价值毋庸置疑。它不仅鉴定出一株具有显著生物钟调节潜力的益生菌菌株,更重要的是建立了一套高效、低成本的体外筛选模型,为未来定向筛选具有特定功能(如抗焦虑、助眠、调节代谢)的益生菌提供了可行的技术路径。
不过,任何补充剂都无法替代健康的生活方式。维持规律的作息、保证充足的睡眠,永远是我们守护生物钟、保持身心健康的第一道也是最根本的防线。
参考资料:
[1]Huang L, Li X, Guo M, Lu W, Zhao J, Xiao Y, Chen W.Bifidobacterium longum supplementation prevents intestinal inflammation and cognitive impairment in sleep-deprived mice by modulating clock gene expression. Food Funct. 2025 Nov 10. doi: 10.1039/d5fo02921j. Epub ahead of print. PMID: 41212119.
原标题:熬夜伤身,但有“后悔药”?江南大学最新:这种益生菌能调节生物钟基因,修复熬夜损伤的肠道屏障,甚至缓解焦虑,提升记忆力
本文作者:木白,转载于微信公众号:梅斯学术(ID:medscinews),转载引用请注明原出处