
睡眠作为生物必需行为,其稳态调控机制一直是神经科学领域的核心问题之一。当动物经历长时间清醒后,会出现持续、巩固且深度的恢复睡眠(RS),但介导这一过程的神经元回路仍不明确。过去研究多聚焦于分子通路(如腺苷、褪黑素等),而对感知和传递睡眠稳态信号的神经回路研究有限。非快速眼动睡眠(NREM)被认为是更具恢复性的睡眠阶段,尽管已有多个NREM促进回路被鉴定(如腹外侧视前区VLPO神经元),但负责 “睡眠需求累积” 的特定神经元集群尚未明确。
近日, 约翰斯·霍普金斯大学Mark N. Wu团队在《Science》上发表了题为 “Sleep need–dependent plasticity of a thalamic circuit promotes homeostatic recovery sleep” 的研究性论文。本研究揭示了丘脑连结核(RE)到未定带(ZI)的神经环路在睡眠稳态调控中的关键作用及其机制。RE中的兴奋性神经元在睡眠剥夺时活性升高,其激活会引发梳理、筑巢等睡眠准备行为,随后产生持续、巩固且深度的非快速眼动(NREM)睡眠,类似稳态恢复睡眠。RE神经元通过向ZI中多个促进非快速眼动睡眠神经元投射发挥作用,睡眠剥夺会诱导RE-ZI连接的神经可塑性变化,这种可塑性与后续稳态恢复睡眠的量相关,且依赖钙/钙调蛋白依赖性蛋白激酶II(CaMKII)。这一发现揭示了睡眠缺失通过改变睡眠环路的功能耦合来促进持续深度睡眠的机制,为理解睡眠稳态调控提供了新视角。

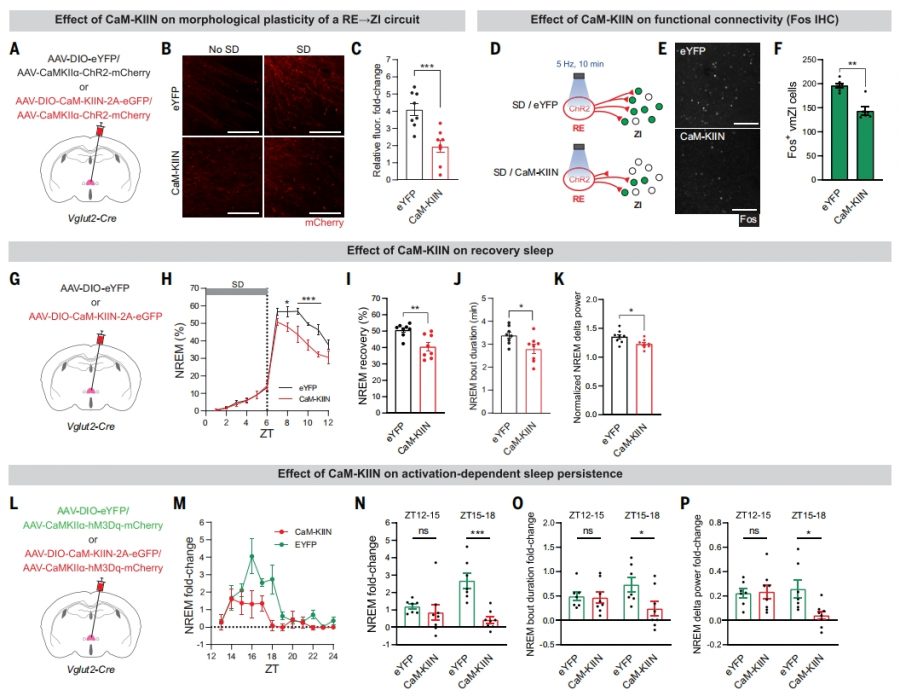
01 RE神经元激活诱导持续性深度NREM睡眠
通过狂犬病毒逆行追踪和化学遗传学筛选,研究团队在小鼠丘脑连结核(RE)中鉴定出一群谷氨酸能神经元(REVglut2),其投射至多个NREM促进脑区(基底前脑、视前区、未定带ZI等)。光遗传激活REVglut2神经元后,小鼠出现独特表型:先表现出筑巢、梳理等睡眠准备行为,约20分钟延迟后进入持续6小时以上的深度NREM睡眠,其delta波功率(睡眠深度标志物)显著升高。这一表型与睡眠剥夺后的稳态恢复睡眠高度相似,提示RE神经元可能参与睡眠稳态调控。
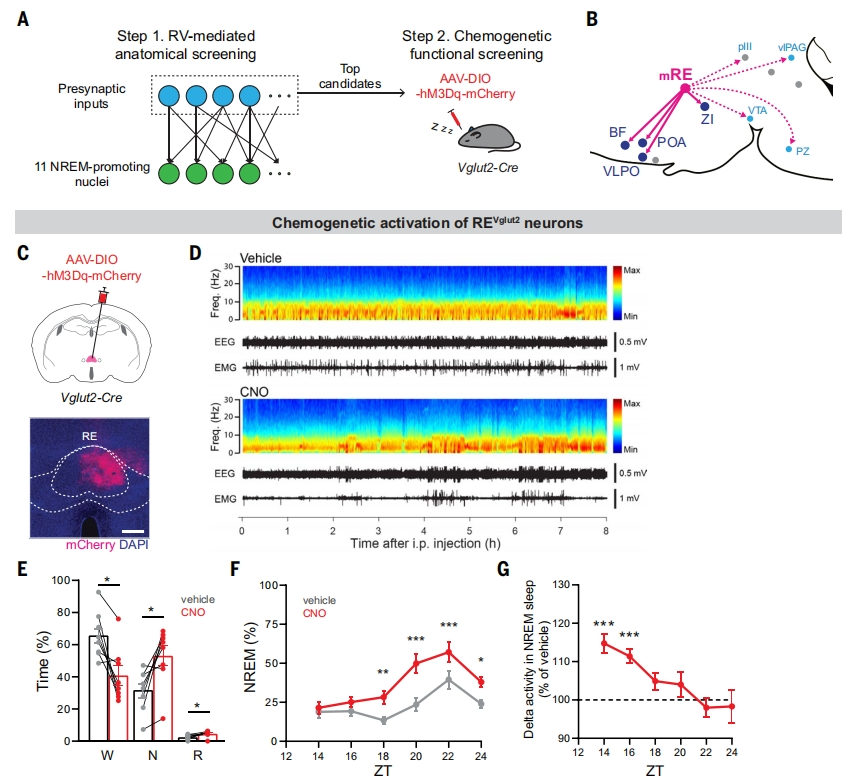
02 RE神经元活动在睡眠剥夺中升高,是稳态恢复的必要条件
Neuropixels电生理记录显示,RE 神经元在睡眠剥夺(SD)期间放电频率显著增加,而在恢复睡眠阶段降低。化学遗传抑制SD期间的RE神经元活性,会导致后续恢复睡眠的时长、巩固性和深度均显著下降。进一步通过TRAP2 系统标记SD激活的RE神经元,发现其电生理兴奋性在SD后增强,且选择性消融这些神经元会损害稳态恢复睡眠。这表明RE神经元的活动是睡眠需求累积的关键环节。
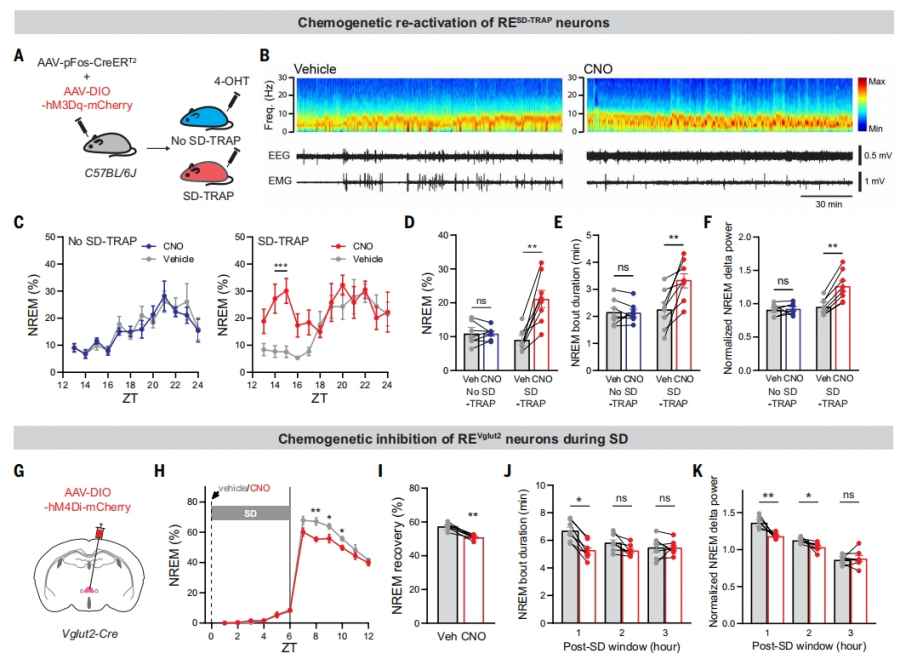
03 RE-ZI回路的可塑性是睡眠需求的分子读码器
REVglut2神经元主要通过投射至未定带(ZI)的Lhx6+神经元发挥作用。SD 诱导RE-ZI 突触的形态和功能可塑性改变:RE 轴突在ZI 区的树突分支和突触前标志物(SYP)数量增加,且这种可塑性与后续恢复睡眠的时长呈正相关。
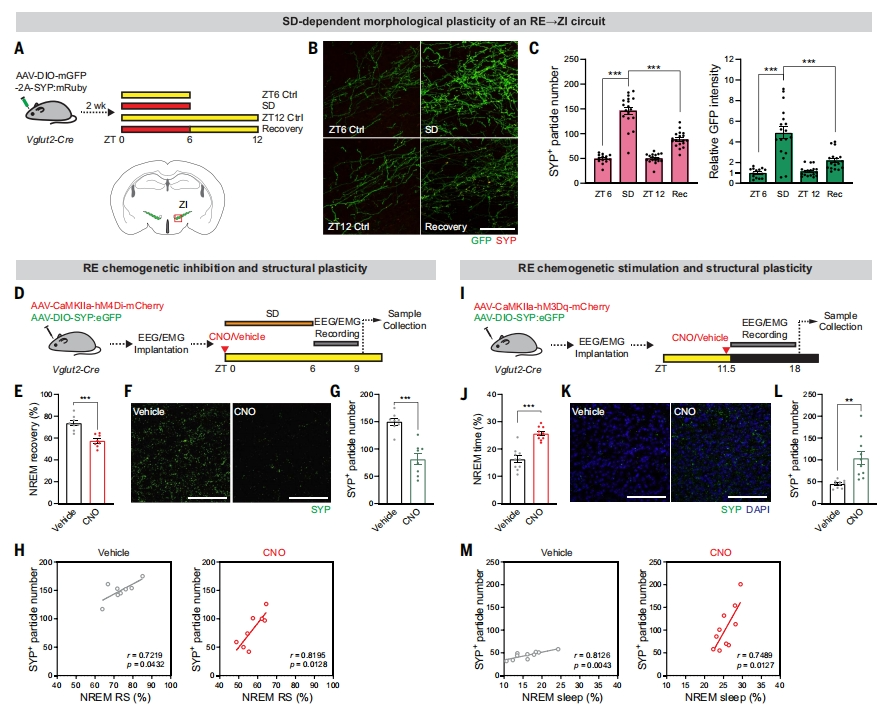
跨突触增强型绿色荧光蛋白重构分析(eGRASP)显示,SD 后RE-ZI 突触连接强度显著提升,电生理记录也证实 SD 增强了两者的功能耦合。
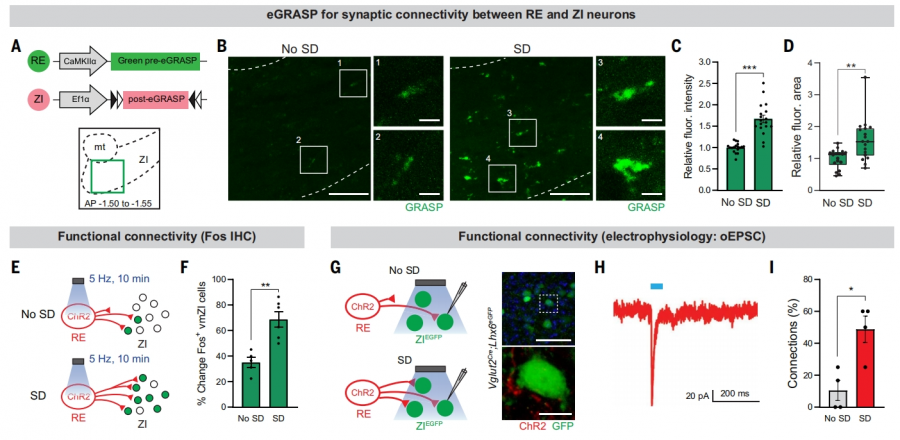
钙/钙调蛋白依赖性蛋白激酶II(CaMKII)在这一过程中起关键作用:抑制 RE 神经元中的 CaMKII 活性会阻断 RE-ZI 可塑性,并削弱恢复睡眠。
04 机制模型:从睡眠需求到回路重塑的闭环调控
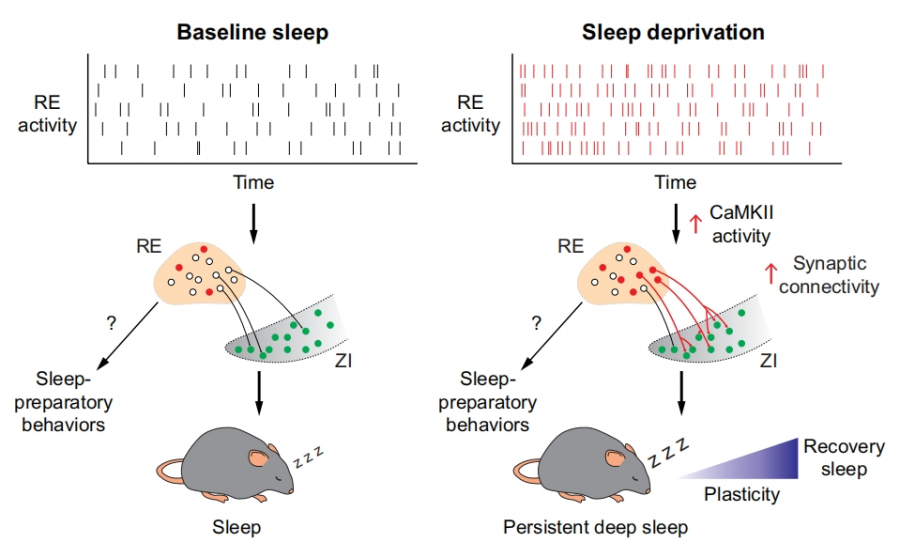
研究提出以下模型:清醒状态下,RE神经元活动增强→激活CaMKII→促进RE-ZI突触结构与功能可塑性改变→增强RE对ZI的信号传递→触发持续性深度恢复睡眠。其中,RE-ZI可塑性的程度直接反映睡眠需求的强度,成为 “睡眠需求的分子读码器”。这一机制通过回路重塑实现睡眠稳态的精准调控,避免过度或不足的睡眠反弹。
05 讨论
本研究揭示的神经回路机制为睡眠稳态调控提供了新的视角。在基线条件下,mREVglut2神经元与睡眠促进的vmZILhx6神经元之间的连接有限且较弱。而睡眠缺失会触发该回路的实质性神经可塑性变化,从而增强其形态和功能连接。这种需求依赖性可塑性需要 CaMKII 的参与,并促进了持续、深沉且巩固的恢复睡眠。
从与现有理论的关系来看,CaMKII 在突触可塑性和睡眠稳态调节中的作用已被广泛研究,本研究进一步证实了其在RE-ZI 回路可塑性中的关键作用,为CaMKII参与睡眠稳态调控提供了新的实验证据。
然而,本研究也存在一定的局限性。尽管研究表明mRE簇在睡眠稳态调节中起着关键作用,但RS并未因mRE功能丧失而完全消失,这提示可能还有其他分子或回路参与其中。此外,虽然短暂的光遗传激活RE神经元可诱导持续性NREM 睡眠,但在如此短的时间内不太可能发生RE-ZI结构可塑性,因此,RE或ZI神经元中可能还存在其他机制促成这一表型。
参考文献:https://doi.org/10.1126/science.adm8203
原标题:Science | 找到了!熬完夜之后睡的更香的神经环路机制!
本文作者:古月,转载于微信公众号:Neurobiology(ID:bukaopuxuezhang),转载引用请注明原出处